
语音播报

TDP-43是一种重要的RNA结合蛋白,其基因突变可引起肌萎缩性侧索硬化症(ALS,俗称“渐冻人症”)。在正常细胞中,TDP-43蛋白主要弥散分布于细胞核内,但可穿梭至胞浆并与其它蛋白相互作用形成应激颗粒等各种核糖核蛋白复合物,参与RNA剪切、成熟、加工、运输、转运、翻译、降解等多个步骤的调控。在疾病状态下,TDP-43在胞浆中形成异常蛋白聚集被认为与ALS的发生发展密切相关。近期研究显示,液-液相分离(LLPS)介导了无膜、液滴状的应激颗粒的生成,而其异常相变被认为是导致胞浆形成TDP-43蛋白聚集并引发ALS的关键致病机制之一。细胞应激时部分TDP-43蛋白被招募到胞浆中参与应激颗粒的组装,但绝大部分的TDP-43依然驻留在细胞核内。目前,核内TDP-43在细胞应激时的反应及其在ALS发病中的作用长期以来被忽视和低估。
近日,中国科学院上海有机化学研究所生物与化学交叉研究中心研究员方燕姗课题组、研究员刘聪课题组合作,研究揭示不同类型的RNA精密调控TDP-43的相分离状态,使其在细胞应激时于核内形成具有细胞保护功能的无膜、液滴状、高度动态且可逆的核颗粒,研究团队将之命名为“TDP-43核体” 。
该研究表明,TDP-43核体通过TDP-43蛋白的液-液相分离所形成,这一过程被RNA严格调控。TDP-43蛋白序列中的两个RNA识别域RRM1和RRM2分别发挥着不同甚至相互拮抗的“向心–离心”作用,因而缺乏RRM1或RRM2的TDP-43核体分别展现出“核”-“环”形态。总RNA对TDP-43蛋白相分离具有抑制作用,这与细胞核中相对“抑制性”的微环境一致,因此很少看到正常细胞自发形成的TDP-43核体。研究发现,细胞应激时神经元中长链非编码RNA (lncRNA) NEAT1 的水平明显升高而且与TDP-43核体共定位。体外实验结果显示,NEAT1可明显促进TDP-43蛋白相分离的发生,下调细胞中NEAT1水平会显著减少应激细胞中TDP-43核体的形成,因此证明NEAT1对于TDP-43形成应激核体具有重要调控作用。
进一步研究发现,与所有其它已知的ALS致病突变主要集中在影响蛋白-蛋白相互作用的功能域不同,TDP-43蛋白的D169G位突变(存在于ALS病人中)位于其RNA识别域RRM1中,并能严重影响lncRNA NEAT1促进TDP-43相分离和核体组装的功能,导致细胞应激时有更多TDP-43蛋白从核内转移至胞浆中,持续应激下进一步发展成具有ALS病理特征的高度磷酸化的TDP-43蛋白聚集体。与此一致的是,D169G突变的TDP-43在人源细胞和果蝇模型中均引起比野生型TDP-43更强的细胞毒性和神经退化的表型。
该研究提示,TDP-43核体的形成或许是细胞应激时的“第一防线”,其组装或功能异常可能与ALS的发生有重要关系。
相关成果以Stress induces dynamic, cytotoxicity-antagonizing TDP-43 nuclear bodies via paraspeckle lncRNA NEAT1-mediated liquid-liquid phase separation为题,发表在Molecular Cell上。研究生王晨、段永嘉和段钢共同第一作者为共同第一作者,方燕姗、刘聪为共同通讯作者。研究得到国家重点研发计划、国家自然科学基金委、中科院和上海市科委的支持。
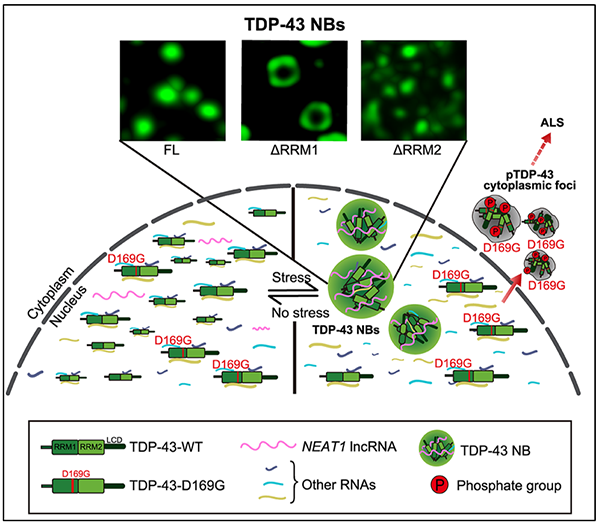
TDP-43核体响应细胞应激和参与ALS疾病发生的分子机制示意图

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)
© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)
© 1996 - 中国科学院 版权所有
京ICP备05002857号-1 京公网安备110402500047号
京公网安备110402500047号
网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话:86 10 68597114(总机)
86 10 68597289(总值班室)
