院况简介
1949年,伴随着新中国的诞生,中国科学院成立。
作为国家在科学技术方面的最高学术机构和全国自然科学与高新技术的综合研究与发展中心,建院以来,中国科学院时刻牢记使命,与科学共进,与祖国同行,以国家富强、人民幸福为己任,人才辈出,硕果累累,为我国科技进步、经济社会发展和国家安全做出了不可替代的重要贡献。 更多简介 +
院领导集体
创新单元
科技奖励
科技期刊
工作动态/ 更多
中国科学院学部
中国科学院院部

语音播报

近期,中国科学院合肥物质科学研究院健康与医学技术研究所戴海明课题组在化疗药物诱导肿瘤细胞焦亡研究方面取得进展。研究人员不仅明确了线粒体外膜蛋白BAK/BAX在化疗药物诱导的细胞焦亡信号通路中的作用,而且首次报道了GSDME Cys407/Cys408棕榈酰化修饰在化疗药物诱导的细胞焦亡过程中的作用。同时,该研究还发现了药物诱导的细胞凋亡和细胞焦亡转换的新机制。相关论文“Chemotherapy-induced Pyroptosis Is Mediated by BAK/BAX-caspase-3-GSDME Pathway and Inhibited by 2-bromopalmitate”发表在Nature出版集团旗下的Cell Death & Disease 杂志上。
细胞焦亡是一种由Gasdermin蛋白家族介导的促炎性程序性细胞死亡方式,主要形态特征包括细胞胀大、细胞膜破裂及细胞吹泡等。先前的研究已经证明该家族的GSDME蛋白的活化是caspase-3依赖的,并且GSDME的表达水平与化疗药物引起的细胞死亡方式密切相关,高表达的GSDME诱导细胞发生焦亡,反之细胞则会走向凋亡。但目前关于GSDME介导细胞焦亡发生的调控研究仍比较匮乏。
该研究使用多种化疗药物处理肿瘤细胞,证明化疗药物引起的细胞焦亡是BAK/BAX-caspase-3-GSDME信号通路依赖的。同时,该研究发现在某些化疗药物引发的细胞焦亡过程中,GSDME的活性受到棕榈酰化修饰的调控,Cys407、Cys408是其潜在的棕榈酰化修饰位点。进一步的研究发现,棕榈酰化修饰可能是通过促进活性GSDME-N从抑制性的GSDME-C上解离来促进细胞焦亡发生的。
该研究不仅充实了化疗药物诱导的肿瘤细胞焦亡信号通路,证明了GSDME的翻译后修饰与其活性的相关性,也为细胞焦亡和细胞凋亡的转换提供了一个新的思路和未来干预的新靶点。研究在方志友课题组、王宏志课题组的协助下完成,受到国家自然基金项目、合肥物质科学技术中心项目资助。
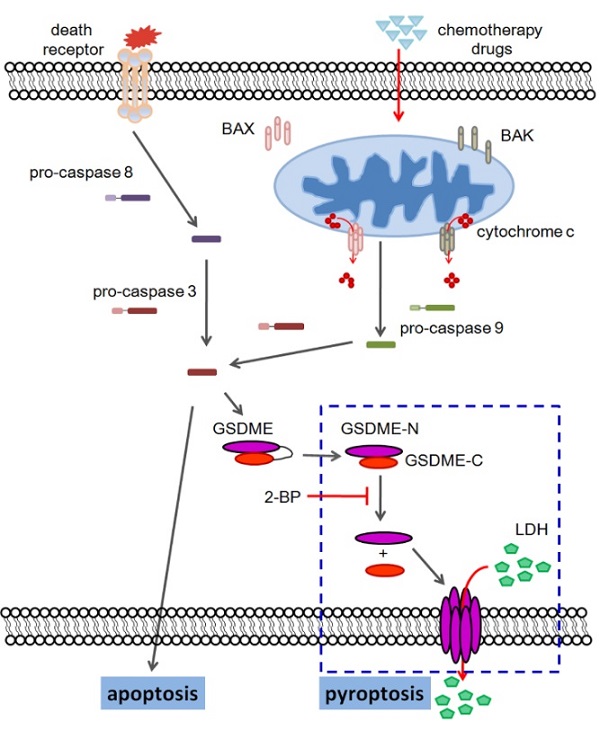
GSDME修饰调控化疗药物诱导的细胞焦亡与细胞凋亡的转化示意图

© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)
© 1996 - 中国科学院 版权所有 京ICP备05002857号-1  京公网安备110402500047号 网站标识码bm48000002
京公网安备110402500047号 网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话: 86 10 68597114(总机) 86 10 68597289(总值班室)
© 1996 - 中国科学院 版权所有
京ICP备05002857号-1 京公网安备110402500047号
京公网安备110402500047号
网站标识码bm48000002
地址:北京市西城区三里河路52号 邮编:100864
电话:86 10 68597114(总机)
86 10 68597289(总值班室)











